Относятся ли гистоны к кислым белкам. Основные белки хроматина - гистоны
К ним относятся гистоны и негистоновые белки.
Гистоны - сильноосновные белки. Их щелочность связана с их обогащенностью основными аминокислотами (главным образом лизином и аргинином). Эти белки не содержат триптофана. Препарат суммарных гистонов можно разделить на 5 фракций :
Н1 (от английского histone) - богатый лизином гистон, мол. Масса 2100;
Н2а - умеренно богатый лизином гистон, масса 13 700;
Н2б - умеренно богатый лизином гистон, масса 14 500;
Н4 - богатый аргинином гистон, масса 11 300;
Н3 - богатый аргинином гистон, масса 15 300.
В препаратах хроматина эти фракции гистонов обнаруживаются в приблизительно равных количествах, кроме Н1, которого примерно в 2 раза меньше любой из других фракций.
Для молекул гистонов характерно неравномерное распределение основных аминокислот в цепи: обогащенные положительно заряженными аминогруппами наблюдается на концах белковых цепей. Эти участки гистонов связываются с фосфатными группировками на ДНК, в то время как сравнительно менее заряженные центральные участки молекул обеспечивают их взаимодействие между собой. Таким образом, взаимодействие между гистонами и ДНК, приводящее к образованию дезоксирибонуклеопротеинового комплекса, носит ионный характер.
Гистоны синтезируются на полисомах в цитоплазме, этот синтез начинается несколько раньше редупликации ДНК. Синтезированные гистоны мигрируют из цитоплазмы в ядро, где и связываются с участками ДНК.
Функциональная роль гистонов не вполне ясна. Одно время считалось, что гистоны являются специфическими регуляторами активности ДНК хроматина, но одинаковость строения основной массы гистонов говорит о малой вероятности этого. Более очевидна структурная роль гистонов, которая обеспечивает не только специфическую укладку хромосомной ДНК, но и играет роль в регуляции транскрипции.
Негистоновые белки - наиболее плохо охарактеризованная фракция хроматина. Кроме ферментов, непосредственно связанных с хроматином (ферменты, ответственные за репарацию, редубликацию, транскрипцию и модификации ДНК, ферменты модификации гистонов и других белков), в эту фракцию входит множество других белков. Весьма вероятно, что часть негистоновых белков представляет собой специфические белки - регуляторы, узнающие определенные нуклеотидные последовательности в ДНК.
РНК хроматина составляет от 0, 2 до 0, 5% от содержания ДНК. Эта РНК представляет собой все известные клеточные типы РНК, находящиеся в процессе синтеза или созревания в связи с ДНК хроматина.
В составе хроматина могут быть обнаружены липиды до 1 % от весового содержания ДНК, их роль в структуре и функционировании хромосом остается неясной.
Хромосомная ДНК упакована в компактную структуру с помощью специализированных белков. Все ДНК-связывающие белки эукариот подразделяются на два класса: гистоны - структурные белки эукариотических хромосом и негистоновые хромосомные белки . Комплекс обоих классов белков с ядерной ДНК эукариотических клеток называется хроматином . Гистоны являются уникальной характеристикой эукариот и присутствуют в огромных количествах на клетку (около 60 миллионов молекул каждого типа на клетку).
Гистоны - относительно небольшие белки с очень большой долей положительно заряженных аминокислот (лизина и аргинина); положительный заряд помогает гистонам крепко связываться с ДНК (которая заряжена сильно отрицательно) независимо от ее нуклеотидной последовательности. Возможно, гистоны только изредка диссоциируют от ДНК и таким образом, вероятно, оказывают влияние на любой процесс, происходящий на хромосомах.
Пять типов гистонов распадаются на две главных группы - нуклеосомные гистоны и Н1 гистоны .
Гистоны образуют семейство высококонсервативных основных белков, которые разделяются на пять больших классов, названных , H2A , H2B , и . Гистоны H1 более крупные (около 220 аминокислот) и оказались менее консервативными в ходе эволюции. Размер полипептидных цепей гистонов лежит в пределах ~220 (H1) и 102 (H4) аминокислотных остатков. Гистон H1 сильно обогащен остатками Lys, для гистонов H2A и H2B характерно умеренное содержание Lys, полипептидные цепи гистонов H3 и H4 богаты Arg. Внутри каждого класса гистонов (за исключением H4) на основании аминокислотных последовательностей различают несколько субтипов этих белков. Такая множественность особенно характерна для гистонов класса H1 млекопитающих. В этом случае различают семь субтипов, названных H1.1-H1.5 , H1o и H1t .Гистоны H3 и Н4 принадлежат к наиболее консервативным белкам. Такая эволюционная консервативность предполагает, что для функции данных гистонов важны почти что все их аминокислоты. N- концевая часть данных гистонов может быть обратимо модифицирована в клетке за счет ацетилирования отдельных остатков лизина, что убирает положительный заряд лизинов.
Резюме: Гистоны (histones) [греч. histos - ткань] - группа небольших по молекулярной массе белков, входящих в состав хроматина). Различают пять основных видов гистонов: H1, H2, H3a, H3b и H4 (Н - от англ. h(istone), а цифры и буквы обозначают номера фракций при их хроматографической очистке). Содержат повышенное количество лизина, гистидина и аргинина, но совсем не содержат триптофан; обладают слабыми щелочными свойствами. Гистоны принадлежат к наиболее консервативным по первичной структуре белкам в ряду от простейших эукариот до высших. Напр., аминокислотные последовательности гистона Н4 из вилочковой железы теленка и проростков гороха различаются только по двум положениям аминокислот из ста двух. Способность гистонов образовывать комплексы определяет чрезвычайно важную их функцию в клеточном ядре: формирование нуклеосомного ядра или кора (от англ. «core» - сердцевина, ядро) - мультибелкового комплекса, вокруг которого накручивается спираль ДНК (см.
Ядерных белков , необходимых для сборки и упаковки нитей в хромосомы . Существует пять различных типов гистонов, названных H1/Н5, H2A, H2B, H3, H4. Последовательность аминокислот в этих белках практически не различается в организмах различного уровня организации. Гистоны - небольшие, сильно основные белки, связывающиеся непосредственно с ДНК. Гистоны принимают участие в структурной организации хроматина , нейтрализуя за счёт положительных зарядов аминокислотных остатков отрицательно заряженные фосфатные группы ДНК, что делает возможной плотную упаковку ДНК в ядре.
Благодаря этому 46 молекул ДНК диплоидного генома человека общей длиной около 2 м, содержащих в сумме 6·10 9 пар оснований (п.о.), могут поместиться в клеточном ядре диаметром всего 10 мкм.
По две молекулы каждого из гистонов Н2А, Н2В, Н3 и Н4 составляют октамер, обвитый сегментом ДНК длиной 146 п.о., образующим 1,8 витка спирали поверх белковой структуры. Эта частица диаметром 7 нм называется нуклеосомой . Участок ДНК (линкерная ДНК), непосредственно не контактирующий с гистоновым октамером, взаимодействует с гистоном Н1.
Группа негистоновых белков высоко гетерогенна и включает структурные ядерные белки, множество ферментов и факторов транскрипции, связанных с определёнными участками ДНК и осуществляющих регуляцию генной экспрессии и других процессов.
Гистоновые белки интересны со многих точек зрения. Благодаря высокому содержанию лизина и аргинина они, как уже упоминалось, проявляют сильно основные свойства. Кроме того, последовательность аминокислот гистонов, то есть их первичная структура, мало изменилась в процессе эволюции. Это хорошо видно при сравнении аминокислотной последовательности гистонов млекопитающих, растений и дрожжей. Так, Н4 человека и пшеницы отличаются лишь несколькими аминокислотами. К тому же размер молекулы белка и её полярность довольно постоянны. Из этого можно заключить, что гистоны были оптимизированы ещё в эпоху общего предшественника животных, растений и грибов (более 700 млн лет назад). Хотя с тех пор в гистоновых генах происходили бесчисленные точковые мутации, все они, очевидно, приводили к вымиранию мутантных организмов.
Гистоны в октамере имеют подвижный N-концевой фрагмент («хвост») из 20 аминокислот, который выступает из нуклеосом и важен для поддержания структуры хроматина и контроля за генной экспрессией. Так, например, формирование (конденсация) хромосом связано с фосфорилированием гистонов, а усиление транскрипции - с ацетилированием в них остатков лизина. Детали механизма регуляции до конца не выяснены.
Некоторые детали механизма регуляции смотри : Белки группы polycomb
Wikimedia Foundation . 2010 .
Роль ДНК в составе как интерфазных хромосом (хроматин интерфазного ядра), так и митотических хромосом достаточно ясна: хранение и реализация генетической информации. Однако для выполнения этих функций в составе интерфазных ядер необходимо иметь четкую структурную основу, которая позволила бы расположить огромные по длине молекулы ДНК в строгом порядке, чтобы с определенной временной последовательностью протекали процессы как синтеза РНК, так и редупликации ДНК В интерфазном ядре концентрация ДНК достигает 100 мг/мл (!). В среднем на интерфазное ядро млекопитающих приходится около 2 м ДНК, которая локализуется в сферическом ядре со средним диаметром около 10 мкм. Это значит, что такая огромная масса ДНК должна как-то быть уложена с коэффициентом упаковки 1 х 10 3 --1 х 10 4 . И при этом в ядре должен сохраниться определенный порядок в расположении частично или полностью деконденсированных хромосом. И кроме того, должны быть реализованы условия для упорядоченного функционирования хромосом. Ясно, что все эти требования не могут быть осуществлены в бесструктурной, хаотической системе.
В клеточном ядре ведущую роль в организации расположения ДНК, в ее компактизации и в регулировании функциональных нагрузок принадлежит ядерным белкам. Как уже указывалось, хроматин представляет собой сложный комплекс ДНК с белками, дезоксирибонуклеопротеин (ДНП), где на долю белков приходится около 60% от сухого веса. Белки в составе хроматина очень разнообразны, но их можно разделить на две группы: гистоны и негистоновые белки . На долю гистонов приходится до 80% от всех белков хроматина. Их взаимодействие с ДНК происходит за счет солевых или ионных связей и неспецифично в отношении состава или последовательностей нуклеотидов в молекуле ДНК. Несмотря на преобладание в общем количестве, гистоны представлены небольшим разнообразием белков: эукариотические клетки содержат всего 5-7 типов молекул гистонов. В отличие от гистонов, т.н. негистоновые белки большей частью специфически взаимодействуют с определенными последовательностями молекул ДНК, очень велико разнообразие типов белков, входящих в эту группу (несколько сот), велико разнообразие функций, которые они выполняют.
Гистоны связаны с ДНК в виде молекулярного комплекса, в виде субъединиц или нуклеосом . До этого считалось, что ДНК равномерно покрыта этими белками, связь которых с ДНК определяется свойствами гистонов.
Гистоны – белки характерные только для хроматина, обладают рядом особых качеств. Это основные или щелочные белки, свойства которых определяются относительно высоким содержанием таких основных аминокислот как лизин и аргинин. Именно положительные заряды на аминогруппах лизина и аргинина обусловливают солевую или электростатическую связь этих белков с отрицательными зарядами на фосфатных группах ДНК. Эта связь достаточно лабильна, легко нарушается, в этом случае может происходить диссоциация ДНП на ДНК и гистоны. Поэтому хроматин, дезоксирибонуклеопротеин или ще как называли раньше, нуклеогистон, является сложным нуклеиново-белковым комплексом, в который входят линейные высокополимерные молекулы ДНК и огромное множество молекул гистонов (до 60 млн. копий каждого типа гистонов на ядро).
Гистоны – наиболее хорошо биохимически изученные белки (см. табл. 5).
Таблица 5 . Общие свойства гистонов млекопитающих
Гистоны – относительно небольшие по молекулярной массе белки. Эти белки практически у всех эукариот обладают сходными свойствами, обнаруживаются одни и те же классы гистонов. Классы гистонов отличаются друг от друга по содержанию разных основных аминокислот. Так гистоны H3 и H4 относят к аргинин-богатым, из-за относительно высокого содержания в них этой аминокислоты. Эти гистоны являются наиболее консервативными из всех исследованных белков: их аминокислотные последовательности практически одинаковы даже у таких отдаленных видов как корова и горох (всего две аминокислотных замены).
Два других гистона H2A и H2B относятся к умеренно обогащенным лизином белкам. У различных объектов внутри этих групп гистонов обнаруживаются межвидовые вариации в их первичной структуре, в последовательности аминокислот.
Гистон H1, представляет собой не уникальную молекулу, а класс белков, состоящих из нескольких достаточно близкородственных белков с перекрывающимися последовательностями аминокислот. У этих гистонов обнаружены значительные межвидовые и межтканевые вариации. Однако их общим свойством является обогащенность лизином, что делает их самыми основными белками, которые легко отделяются от хроматина в солевых (0,5 М) растворах. В растворах с высокой ионной силой (1-2 М NaCI) все гистоны полностью отделяются от ДНК и переходят в раствор.
Для гистонов всех классов (особенно для H1) характерно кластерное распределение основных аминокислот, лизина и аргинина, на N- и C-концах молекул. Срединные участки молекул гистонов образуют несколько (3-4) -спиральных участка, которые компактизуются в глобулярную структуру в изотонических условиях (рис. 56). По-видимому, богатые положительными зарядами неспирализованные концы белковых молекул гистонов и осуществляют их связь друг с другом и с ДНК.
У гистона H1 наиболее вариабельным является N-конец, осуществляющий связь с другими гистонами, а C-конец, богатый лизином, взаимодействует с ДНК.
В процессе жизнедеятельности клеток могут происходить посттрансляционные изменения (модификации) гистонов: ацетилирование и метилирование некоторых остатков лизина, что приводит к потере числа положительных зарядов, и фосфорилирование сериновых остатков, приводящее к появлению отрицательного заряда. Ацетилирование и фосфорилирование гистонов может быть обратимым. Эти модификации значительно меняют свойства гистонов, их способность связываться с ДНК. Так повышенное ацетилирование гистонов предшествует активации генов, а фосфорилирование и дефосфорилирование связаны соответственно с конденсацией и деконденсацией хроматина.
Гистоны синтезируются в цитоплазме, транспортируются в ядро и связываются с ДНК во время ее репликации в S-периоде, т.е. синтез гистонов и ДНК синхронизированы. При прекращении клеткой синтеза ДНК гистоновые информационные РНК за несколько минут распадаются и синтез гисонов останавливается. Включившиеся в хроматин гистоны очень стабильны, имеют низкую скорость замены.
Подразделение гистоноы на пять групп и достаточное сходство их внутри каждой группы в целом характерно для эукариот. Однако целый ряд отличий в составе гистонов наблюдается как у высших, так и у низших эукариотических организмов. Так у низших позвоночных вместо H1, характерного для всех тканей этих организмов, в эритроцитах находят гистон H5, который содержит больше аргинина и серина. С другой стороны, наблюдается отсутствие некоторых групп гистонов у ряда эукариот, и в целом ряде случаев полная замена этих белков на другие.
Гистоноподобные белки были обнаружены в составе вирусов, бактерий, митохондрий. Так, например, у E. coli в клетке в большом количестве обнаруживаются белки (HU и H-NS), по аминокислотному составу напоминающие гистоны.
Функциональные свойства гистонов
Широкое распространение гистонов, их сходство даже у очень отдаленных видов, обязательность вхождения их в состав хромосом, все это говорит об их чрезвычайно важной роли в процессе жизнедеятельности клеток. Еще до открытия нуклеосом существовало две взаимодополняющие друг друга группы гипотез о функциональной роли гистонов, о регуляторной и структурной их роли.
Было обнаружено, что выделенный хроматин при добавлении к нему РНК-полимеразы может быть матрицей для транскрипции, однако активность его составляет всего лишь около 10% от активности, соответствующей активности выделенной чистой ДНК. Эта активность прогрессивно возрастает по мере удаления групп гистонов и может достичь 100% при полном удалении гистонов. Отсюда можно было сделать вывод, что общее содержание гистонов может регулировать уровень транскрипции. Это наблюдение совпадает с тем, что по мере удаления гистонов, особенно H1, происходит прогрессивная деконденсация, разворачивание фибрилл ДНП, что возможно облегчает взаимодействие РНК-полимеразы с матричной ДНК. Так же было обнаружено, что модификация гистонов приводит к усилению транскрипции и одновременной декомпактизации хроматина. Следовательно, напрашивается вывод о том, что количественное и качественное состояние гистонов влияет на степень компактности и активности хроматина. Однако оставался открытым вопрос о специфичности регуляторных свойств гистонов: какова роль гистонов при синтезе специфических иРНК в различно дифференцированных клетках. Этот вопрос до сих пор еще не решен, хотя можно сделать некоторые обобщения: на эту роль могут претендовать те группы гистонов, которые наименее консервативны, такие как H1 или как H2A и H2B, которые могут в значительной мере модифицироваться и тем самым изменять свои свойства в определенных участках генома.
Была очевидна и структурная, компактизирующая, роль гистонов в организации хроматина. Так постепенное добавление фракции гистонов к растворам чистой ДНК приводит к выпадению в осадок комплекса ДНП, и наоборот, частичное удаление гистонов из препаратов хроматина, ведет к его переходу в растворимое состояние. С другой стороны, в цитоплазматических экстрактах ооцитов земноводных или яиц морских ежей, содержащих свободные гистоны, добавление любой ДНК (включая фаговую) привводит к образованию хроматиновых фибрилл (ДНП), длина которых в несколько раз короче исходных ДНК. Эти данные говорят о структурной, компактизирующей роли гистонов. Для того, чтобы огромные сантиметровые молекулы ДНК уложить по длине хромосомы, имеющей размер всего несколько микрометров, молекула ДНК должна быть как-то скручена, компактизована с плотностью упаковки равной 1: 10000. Оказалось, что в процессе компактизации ДНК существуют несколько уровней упаковки, первые из которых прямо определяются взаимодействием гистонов с ДНК.
Первый уровень компактизации ДНК: структурная роль нуклеосом
В ранних биохимических и электронномикроскопических работах было показано, что препараты ДНП содержат нитчатые структуры с диаметром от 5 до 50 нм. Постепенно стало ясно, что диаметр фибрилл хроматина зависит от способа выделения препарата.
На ультратонких срезах интерфазных ядер и митотических хромосом после фиксации глутаровым альдегидом обнаруживались хроматированные фибриллы толщиной 30 нм. Такие же размеры имели фибриллы хроматина при физической фиксации ядер - при быстром замораживании ядер, скалывании объекта и получении реплик с таких препаратов. В последнем случае исключалось воздействие на хроматин переменных химических условий. Но все эти методы и приемы не давали никакой информации о характере локализации ДНК и гистонов в хроматиновых фибриллах.
Крупным событием в изучении хроматина было открытие двумя разными способами нуклеосом - дискретных частиц хроматина. Так при осаждении на подложку для электронной микроскопии препаратов хроматина в щелочных условиях при низкой ионной силе, можно было видеть, что нити хроматина представляли собой что-то, напоминающее “бусы на нитке”: небольшие, около 10 нм, глобулы, связанные друг с другом отрезками ДНК длиной около 20 нм (рис. 57, 58). Эти наблюдения совпадали с результатами фракционирования хроматина после частичного нуклеазного переваривания.
Было найдено, что если подвергнуть действию нуклеазы микрококков выделенный хроматин, то он подвергается распаду на регулярно повторяющиеся структуры. Так ДНК, полученная из хроматина, обработанного нуклеазой, состояла из серии отрезков, кратных 200 парам оснований; встречались отрезки в 200, 400, 600, 800 и больше пар нуклеотидов (п.н.). Это говорит о том, что нуклеазной атаке в составе хроматина подвергаются участки ДНК, расположенные примерно через каждые 200 п.н. При этом в кислоторастворимую фракцию (низкополимерная) ДНК уходит всего 2% ядерной ДНК. Кроме того после такой нуклеазной обработки из хроматина путем центрифугирования удается выделить фракцию частиц со скоростью седиментации 11S (S - единица Сведберга, определяющая скорость седиментации частиц, равна 1 х 10 -13 с), а также частицы кратного этой величине размера: димеры, тримеры, тетрамеры и т.д. Оказалось, что частицы 11S содержат ДНК около 200 п.н. и восемь гистонов (октамер ) по две копии гистонов H2A, H2B, H3 и H4 и одну копию гистона H1. Такая сложная нуклеопротеидная частица получила название нуклеосомы . Более подробный анализ этой фракции показал, что нуклеосома устроена следующим образом: октамер гистонов образует белковую основу-сердцевину (от англ. core, часто в нашей литературе этот термин используется без перевода: кор, коровая частица), по поверхности которой располагается ДНК величиной в 146 п.н., образующая 1,75 оборота; остальные 54 п.н. ДНК образуют участок, несвязанный с белками сердцевины - линкер , который, соединяя две соседние нуклеосомы, переходит в ДНК следующей нуклеосомы. Гистон H1 связывается частично с основной, сердцевиной и с участком линкера (около 30 п.н.). Следовательно, полная нуклеосома содержит около 200 п.н. ДНК (146 п.н.- сердцевина, 30 п.н. - участок линкера в комплексе с гистоном H1, 30 п.н. - свободная ДНК), октамер сердцевинных (коровых) гистонов и одну молекулу гистона H1 (рис. 59). Молекулярная масса полной нуклеосомы - 262000 Да. Рассчитано, что на весь гаплоидный геном человека (3 х 10 9 пар оснований) приходится 1,5 х 10 7 нуклеосом.
Сердцевина или коровая частица (или минимальная нуклеосома) очень консервативны по своей структуре: они всегда содержат 146 п.н. ДНК и октамер гистонов. Линкерный участок может значительно варьировать (от 8 до 114 п.н. на нуклеосому).
Используя метод рассеяния нейтронов удалось установить форму и точные размеры нуклеосом. При грубом приближении – это плоский цилиндр или шайба диаметром 11 нм и высотой 6 нм. Располагаясь на подложке для электронного микроскопирования они образуют «бусины», глобулярные образования около 10 нм, гуськом, тандемно сидящие на вытянутых молекулах ДНК. На самом же деле вытянутыми являются только линкерные участки, остальные три четверти длины ДНК спирально уложены по периферии гистонового октамера. Сам гистоновый октамер, как считают, имеет форму, напоминающую мяч для игры в рэгби, в состав которого входит тетрамер (H3 H4) 2 и два независимых димера H2A H2B. На рис. 60 представлена схема расположения гистонов в сердцевинной части нуклеосомы.
В фибриллах хроматина линкерный участок не линеен, а продолжая спираль ДНК на поверхности нуклеосомной частицы,связывает соседние нуклеосомы так, что образуется как бы сплошная нить, толщиной около 10 нм, состоящая из тесно расположенных нуклеосом (рис. 61). При этом за счет дополнительной спирализации ДНК (1 отрицательный супервиток ДНК на 1 нуклеосому) происходит первичная компактизация ДНК, с плотностью упаковки равной 6-7 (200 п.н. длиной 68 нм, уложены в глобулу диаметром 10 нм). Укладка почти двух витков ДНК по периферии сердцевин нуклеосомы происходит, как считается, за счет взаимодействия положительно заряженных аминокислотных остатков на поверхности октамера гистонов с фосфатами ДНК. N- и C-концевые участки сердцевинных гистонов, обогащенные положительными зарядами, вероятно, служат для дополнительной стабилизации структуры нуклеосомы.
Ведущая роль сердцевинных (коровых) белков в компактизации ДНК показана при самосборке нуклеосом. Регулируя последовательность добавления гистонов и ДНК, удалось получить полную реконструкцию нуклеосом. В этом процессе не играет никакой роли источник, откуда была взята ДНК: это может быть ДНК бактерии и даже циклическая ДНК вирусов. Оказалось, что для образования нуклеосом гистон H1 не требуется, он участвует в связывании уже готовых нуклеосом друг с другом и в образовании более высоких уровней компактизации ДНК. Ключевыми в построении нуклеосом оказались гистоны H3 и H4. При этом вначале ДНК связывается с тетрамером (H3 H4) 2 к которому позжеприсоединяются два димера H2A H2B. Вероятно, высокая консервативность в строении гистонов H3 и H4 отражает их ведущую структурную роль на первых этапах компактизации ДНК при образовании нуклеосом.
Белки, связанные с ДНК эукариотов и отличающиеся от гистонов, называют негистоновыми хромосомными белками (НГБ). Они были открыты в 1946 г. Мирским и Поллистером . От ДНК их отделяют с помощью смеси 2 М NaCl и 5 М мочевины. К ним относятся белки, ответственные за экспрессию и репрессию генов хроматина, а также за метаболизм и модификации хромосомных белков . Они имеют изоэлектрические точки от 3,7 до 9,0. Эти белки весьма неоднородны по размеру - их молекулярная масса может составлять от ~8000 до нескольких сотен тысяч. Период полужизни НГБ сильно варьирует, но в целом он много короче, чем у гистонов. Как и гистоны, они синтезируются в цитоплазме и затем переходят в ядра, где образуют комплексы с ДНК . Если ввести НГБ в цитоплазму, они быстро проникают в ядра . Клетки с более высокой метаболической активностью содержат большее количество НГБ, и этим последние отличаются от гистонов, содержание которых одинаково в клетках всех типов. НГБ присутствуют в хроматине всех тканей, но структура их в разных тканях различна как в количественном, так и в качественном отношении, т. е. эти белки ткане- и видоспецифичны. С помощью методов с высоким разрешением показано, что в каждой ткани имеются сотни типов НГБ. В глиальных клетках с помощью изоэлектрофокусирования и микродиск-электрофореза было обнаружено почти 1500 НГБ . По всей вероятности, некоторые из них представляют собой модифицированные НГБ, причем они синтезируются в течение всего клеточного цикла, тогда как гистоны синтезируются только в S-фазе.
После обработки хроматина тимуса теленка 0,3 М NaCl НГБ по подвижности в геле делятся на две группы: высокоподвижная группа (HMG, от англ. high mobility group) с мол. массой менее 30000 и малоподвижная группа с мол. массой более 30000 . К HMG-белкам относятся четыре белка с большим зарядом: HMG 1 HMG 2 , HMG 14 и HMG 17 . Они включают 25 % основных и 30 % кислотных остатков и составляют только 3 % веса ДНК; они присутствуют во всех тканях и не являются тканеспецифичными . Белки HMG ассоциированы с нуклеосомой . Белки HMG 1 и HMG 2 имеют мол. массу около 26000. Они взаимодействуют с ДНК своими основными остатками . Около 50 % остатков HMG 1 заряжены. Необычным является то, что его COOH-концевая область содержит последовательность из 41 чередующихся остатков аспарагиновой и глутаминовой кислот. Каждое ядро из тимуса теленка содержит ~10 6 молекул белков HMG 1 . По-видимому, белки HMG играют в хроматине структурную, а не регуляторную роль. Белок HMG 1 в отличие от трех остальных не содержит ароматических аминокислот. Он включает последовательность из 89 остатков и имеет мол. массу 9247. Его карбоксильный конец представляет собой цепь кислотных остатков, а NH 2 -конец - цепь основных остатков; центральная область богата остатками лизина. HMG 17 не имеет вторичной и третичной структуры, а по последовательности входящих в него аминокислотных остатков он гомологичен гистонам Н1 и Н5. Его уникальная первичная структура с цепями кислотных и основных остатков указывает на то, что он может быть структурным белком. Показано, что белок HMG 17 связывается приблизительно с 57 нуклеотидами ДНК из тимуса теленка и вызывает конформационные изменения в ДНК, сходные с теми, которые производит гистон Н1 , причем с ДНК связываются остатки с 15 по 40 .
Поскольку белки HMG имеют кислотные и основные остатки, образующие кластеры, они могут связываться с гистонами. своими кислотными группами, а с ДНК - основными остатками. Белки HMG 1 и HMG 2 ассоциированы с нуклеосомой . Они стабилизируют двойную спираль ДНК, поскольку при ассоциации с ними ее Т m увеличивается на 20 °C . Таким образом, имеются достаточные основания полагать, что белки HMG играют в хроматине структурную роль. При воздействии ДНКазы I на активную часть хроматина белки HMG удаляются. По-видимому, эти белки связаны с нуклеосомами . Дефер и др. также сообщают, что НГБ связаны с нуклеосомами. Существуют экспериментальные доказательства структурной роли некоторых НГБ . Метафазные хромосомы клеток HeLa сохраняют свою морфологию даже после того, как удалены все гистоны и большинство НГБ. Структура поддерживается лишь с помощью ~30 % НГБ, причем в их число входит около 30 типов НГБ с мол. массой ~75000. Каждая хроматида находится в спаренном состоянии, как в метафазе, и остается стабильной даже в 2 М NaCl. Установлено также, что после удаления гистонов из метафазных хромосом их общий размер уменьшается на 50 %, и это не приводит к заметным нарушениям в их морфологии . Отсюда следует, что НГБ ответственны за поддержание метафазной структуры хромосом, а, возможно, также и структур других фаз клеточного цикла. Есть сообщения , что НГБ участвуют в процессе закручивания ДНК в сверхспираль и в образовании структуры хроматина высшего порядка. В связи с этим было высказано предположение, что НГБ образуют "строительные леса", или каркас, определяя таким образом основную форму метафазной хромосомы , и в соответствии с этим каркасом ДНК сворачивается в петли.
НГБ очень неоднородны, число их велико, и некоторые из них ткане- и видоспецифичны. Общее содержание НГБ в разных тканях соответствует следующему ряду: мозг>печень>>почки>>селезенка>тимус . Некоторые НГБ специфичны для каждой ткани, а относительные количества индивидуальных НГБ варьируют от ткани к ткани. Они претерпевают количественные и качественные изменения при различных физиологических условиях, а также в процессе эмбриогенеза, дифференцировки клеток и клеточного цикла. Некоторые НГБ слабо связаны с ДНК и легко экстрагируются, другие связаны сильнее. Благодаря своим свойствам они участвуют в регуляции экспрессии генов в целом и в контроле транскрипции в частности . Показано , что фракция НГБ из печени крысы стимулирует транскрипцию in vitro. Когда НГБ добавляют к хроматину эмбриона морского ежа, увеличивается число участков инициации синтеза РНК . Аналогичные наблюдения сделаны на клетках асцитного рака Эрлиха: фракция слабо связанных НГБ избирательно ассоциирует с гомологичной ДНК и стимулирует транскрипцию специфических структурных генов в присутствии РНК-полимеразы эукариот . Удалось идентифицировать фосфорилированный НГБ с мол. массой 11000, который ингибирует инициацию транскрипции и играет регуляторную роль в экспрессии генов. Сообщалось также об участии в регуляции специфической активности генов сильно связанных НГБ . Катино и др. изолировали НГБ с мол. массой 31000, который в большом количестве содержится в неделящихся клетках, но в малом количестве - в делящихся, как, например, в гепатоме Новикова. Когда НГБ выделяли из хроматина с помощью 5 М мочевины (М 0), смеси 5 М мочевины и 1 М NaCl (M 1) и смеси 5 М мочевины и 3 М NaCl (M 3) и изучали роль каждой полученной фракции в транскрипции комплекса ДНК - гистон из печени кролика, оказалось, что функции этих трех фракций различны . Фракция М 0 стимулирует транскрипцию, связываясь с хроматином и изменяя общую конформацию комплекса ДНК - гистон. Фракция М 3 связывается более специфическим образом и раскрывает новые центры для связывания РНК-полимеразы. Фракция M 1 включает, по-видимому, структурные компоненты хроматина.
Метаболически более активные клетки содержат большее число НГБ. Обычно НГБ локализованы в тех областях хроматина, которые более активны в процессе синтеза РНК . НГБ способны прекращать репрессию матричной активности, вызываемую гистонами . Некоторые фосфорилированные НГБ специфически взаимодействуют с гистонами Н1 и Н2В и поэтому могут удалять их и открывать участки ДНК для транскрипции . НГБ способны переводить неактивные покоящиеся клетки, находящиеся в фазе G 0 , в активно растущие в стадии G 1 . В процессе этого перехода происходит синтез специфических типов НГБ и одновременно увеличивается матричная активность . Отсюда был сделан вывод, что эти белки участвуют в дерепрессии или в положительной регуляции экспрессии генов, особенно в контроле транскрипции в течение клеточного цикла.
При введении цыпленку эстрадиола или прогестерона синтез НГБ в яйцеводе стимулируется. НГБ в яйцеводе крыс, принимавших гормональные препараты, качественно отличны от белков контрольных животных . Полагают, что в ядре акцептором для прогестерон-рецепторного комплекса является НГБ. Глюкокортикоид-рецепторный комплекс лучше связывается с хроматином печени, чем с хроматином тимуса, простаты и матки. Если из хроматина удалить гистоны, то в оставшемся хроматине связывание комплекса увеличивается вдвое. Если же удалить все хромосомные белки, то связывание рецепторного комплекса глюкокортикоида с ДНК уменьшается на 50 %. Отсюда следует, что НГБ ответственны за связывание рецепторного комплекса гормона с ДНК . Синтез НГБ стимулируется кортизоном и глюкагоном . Стероидные гормоны, индуцирующие фосфорилирование НГБ в яйцеводе , а также кальцитонин и гормоны паращитовидной железы, которые оказывают противоположное действие на метаболизм кальция в костных клетках, стимулируют фосфорилирование различных НГБ .
Экдизон - стероидный гормон, ответственный за развитие насекомых - вызывает образование пуффов в хромосомах слюнных желез у личинок Sciara . Возникновение пуффа указывает на то, что в данном участке происходит транскрипция. В месте пуффа, вызванного действием экдизона, не наблюдается увеличения содержания гистонов или ДНК, в то время как содержание НГБ почти удваивается. Пуффы образуются лишь после окончания определенной стадии развития, когда клетки становятся компетентными (17-дневные личинки); они не появляются у 4-дневных личинок. Это свидетельствует о том, что для действия экдизона необходим какой-то цитоплазматический фактор, вероятно белок. Следовательно, прежде чем экдизон сможет оказать воздействие на специфические гены, должен быть активирован определенный ген, ответственный за синтез этого белка. При возникновении пуффов в политенных хромосомах Drosophila отношение белков к ДНК увеличивается с 6 до 16, количество РНК увеличивается вдвое, а Т m данного участка понижается на 10 °C . Кроме того, около пуффов накапливаются НГБ. В содержании ДНК и гистонов, связан дается никаких изменений, а большая часть гистонов, связанных с ДНК, оказывается дестабилизированной. Эти наблюдения подтверждаются результатами, полученными с помощью иммунофлуоресценции, согласно которым пуффы, индуцированные в политенных хромосомах Drosophila тепловым ударом, содержат новые НГБ. Очевидно, НГБ ответственны за активацию генов.
Воздействие НГБ на экспрессию специфических генов изучалось рядом исследователей . Когда НГБ клеток HeLa добавляли к хроматину этих клеток в фазе G 1 , начиналась транскрипция генов гистонов, хотя обычно в этой фазе их экспрессии нет. При воссоединении хроматина в S-фазе клеток W1-38 с S-фазными НГБ наблюдается 500-кратная стимуляция транскрипции генов гистонов, в то же время при воссоединении хроматина печени мыши с S-фазными НГБ клеток HeLa транскрипции генов глобина не происходит. Эксперименты по реконструкции с использованием хроматина эритроцитов цыпленка показали: для того чтобы вызвать транскрипцию генов глобина, определенная фракция НГБ должна связываться с ДНК раньше, чем с гистоном . После того как удалось разделить хроматин клеток тимуса теленка и костного мозга на ДНК, гистоны и НГБ, полученные компоненты были использованы в опытах по реконструкции . Оказалось, что в случае клеток тимуса синтезированные РНК похожи на РНК тимуса, а мРНК глобина не синтезируются. Когда же был реконструирован и использован для транскрипции хроматин костного мозга, мРНК глобина синтезировались. Вместе с тем если в реконструкции участвовали ДНК и гистон тимуса и НГБ костного мозга, то также происходил синтез мРНК глобина. Отсюда следует, что НГБ, вероятно, участвуют в регуляции специфических генов. В культуре клеток мышц НГБ активно фосфорилируются главным образом во время дифференцировки . Установлено также, что НГБ принимают участие в положительном контроле экспрессии генов. Однако для того, чтобы идентифицировать специфические компоненты НГБ, участвующих в контроле, и установить точный механизм контроля, необходимы дальнейшие исследования.
| <<< Назад
|
Вперед >>>
|
Последние материалы сайта
Обществознание

Начало княжения святослава, сына игорева
По потопе трое сыновей Ноя разделили землю – Сим, Xaм, Иaфeт. И достался восток Симу: Персия, Бактрия, даже и до Индии в долготу, а в ширину до Ринокорура, то есть от востока и до юга, и Сирия, и Мидия до реки Евфрат, Вавилон, Кордуна, ассирияне, Месопота
Технология

К чему снится Герой? Герой войни
В снах мужчины.В снах женщины Анимус.Героические поиски сакрального образа, без его убийства.Сознательное эго, борющееся с силами бессознательного.Существует большое число мифов, в которых герой убивает тёмное и злобное, но делая это, он также уничтожает
Информатика

Тесты для самотестирования
Теоретическая и практическая психология - наука невероятной глубины, позволяющая познать тайны человеческого сознания. Это наука никогда не останавливается и совершенствуется с каждым днем, все больше и больше углубляясь в изучение человеческой личности и
История
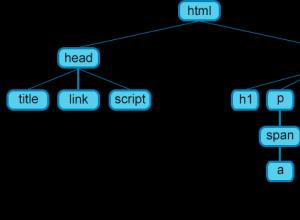
HTML: основы для начинающих Обучение языку html для начинающих
Основы HTML содержат основные правила языка HTML, описание структуры HTML-страницы, отношения в структуре HTML-документа между HTML-элементами. HTML-документ - это обычный текстовый документ, может быть создан как в обычном текстовом редакторе (Блокнот)
Технология
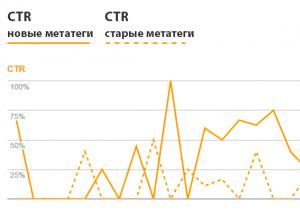
META-тег Keywords — ключевые слова и их значение для поисковых систем Мета тег краткое описание
Настройка Meta-тегов и ключевых слов Приветствую, друзья! В этой статье речь пойдет о том, как писать мета теги. Теги являются неотделимой частью в оптимизации и раскрутке сайта. И им необходимо уделять не меньше внимания, чем другим пунктам оптимизации.